|
Колебательная часть термодинамических величин газа становится существенной при значительно более высоких температурах,
чем
вращательная, потому что интервалы колебательной структуры термов велики по сравнению с интервалами вращательной структуры).
Мы будем считать, однако, температуру большой лишь настолько, чтобы были возбуждены в основном не слишком высокие колебательные уровни. Тогда колебания являются малыми (а потому и гармоническими), и уровни энергии определяются обычным выражением
Ћω(v+1/2) использованным в (4).
Вычисление колебательной статистической суммы Zкол (4) производится элементарно. Вследствие очень быстрой сходимости ряда суммирование можно формально распространить до v = оо. Условимся
Рис. 2.
отсчитывать энергию молекулы от наиболее низкого (v=0) колебательного уровня (т. е. включаем ћω/2 в постоянную ε0 в (1)).
Тогда имеем:
(21)
(22)
(23)
(24)
На рис. 2 изображен график зависимости Скол от T/ћω.
При низких температурах (ћω>>T) все эти величины стремятся экспоненциально к нулю:
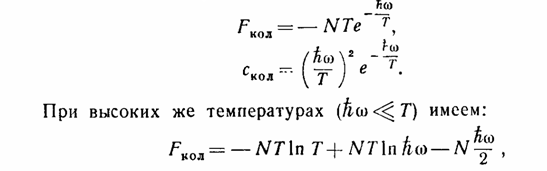
чему соответствует постоянная теплоемкость Скол=1) и химическая постоянная ξкол=-lnћω. Складывая со значениями (11), (12), найдем, что при температурах T>>ћω полная теплоемкость двухатомного газа равна)
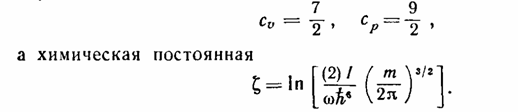
(27)
(28)
В этой формуле для молекул из одинаковых атомов множитель [(2)] должен быть опущен. Первые два члена разложения Eкол равны
(29)
Появление здесь постоянного члена — 1/2Nћω связано с тем, что, мы отсчитываем энергию от низшего квантового уровня (т. е. от энергии «нулевых колебаний»), между тем как классическая энергия должна была бы отсчитываться от минимума потенциальной энергии.
Выражение (26) для свободной энергии можно, конечно, получить и классическим путем, поскольку при T>>ћω существенны большие квантовые числа V, для которых движение квазиклассично. Классическая энергия малых колебаний с частотой ω имеет вид
(т'—приведенная масса). Интегрирование с этим выражением для ε даст для статистического интеграла значение
Перейти на страницу: 1 2 3 |